Комбинированная вакцина против гриппа и ковид-19 компании Moderna достигла прогресса; компания объявила о «положительных данных»
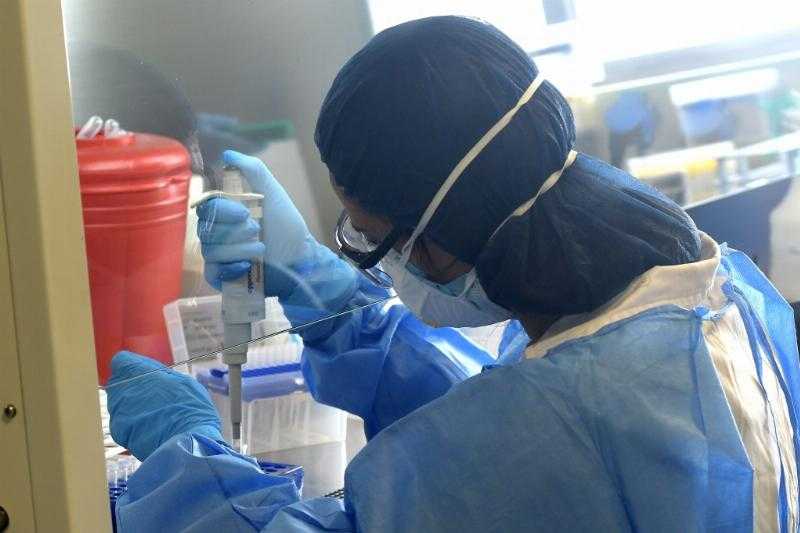
Компания Moderna, производящая вакцины, объявила в понедельник, что испытания третьей фазы мРНК-1083, исследовательской комбинированной вакцины против гриппа и ковид-19, «достигли первичных конечных точек» и «вызвали более высокий иммунный ответ, чем лицензированные вакцины, использованные в испытании». «Комбинированные вакцины способны снизить нагрузку на системы здравоохранения и аптеки, связанную с респираторными вирусами, а также предложить людям более удобные варианты вакцинации, что может обеспечить более надежную защиту от сезонных заболеваний», - сказал Стефан Бансель, главный исполнительный директор компании Moderna. В состав мРНК-1083 входят компоненты мРНК-1010, кандидатной вакцины компании «Модерна» против сезонного гриппа, и мРНК-1283, вакцины нового поколения компании «Модерна» против ковид-19. Каждая из исследуемых вакцин независимо друг от друга продемонстрировала положительные результаты в клинических испытаниях фазы 3. Клиническое испытание фазы 3 «представляет собой активное контрольное, рандомизированное, слепое исследование, оценивающее безопасность, реактогенность и иммуногенность мРНК-1083 в двух независимых возрастных группах, состоящих примерно из 4000 взрослых в каждой», - говорится в сообщении Moderna. Одна когорта состоит из людей в возрасте 65 лет и старше. В этой группе мРНК-1083 сравнивали с Fluzone HD, усиленной противогриппозной вакциной, и Spikevax®, лицензированной в настоящее время вакциной Moderna против ковид-19. В другой части испытания исследователи сравнили результаты применения мРНК-1083 у взрослых в возрасте 50-64 лет с совместным применением Fluarix®, стандартной дозы вакцины против гриппа, и Spikevax. Исследователи обнаружили, что «иммунный ответ на однократную дозу мРНК-1083 был не хуже, чем у лицензированных аналогов». Кроме того, в обеих группах «мРНК-1083 также вызывала статистически значимо больший иммунный ответ против трех штаммов вируса гриппа (H1N1, H3N2 и B Victoria) и против SARS-CoV-2». "МРНК-1083 продемонстрировал приемлемый профиль безопасности и переносимости. Большинство зарегистрированных побочных реакций были 1 или 2 степени тяжести и соответствовали лицензированным вакцинам, использованным в испытании. Наиболее часто сообщалось о таких побочных реакциях, как боль в месте инъекции, усталость, миалгия и головная боль", - заявила разработчик вакцины. Компания Moderna планирует представить клинические данные этой фазы исследования на своей следующей медицинской конференции и отправить их для публикации.